-
미리보기
소개
"용해도곱 상수 결정"에 대한 내용입니다.목차
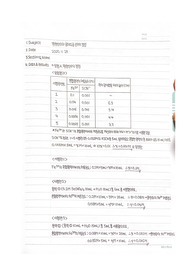
1. 실험 결과 분석
2. 실험 결과에 대한 고찰
3. 토의
4. 참고문헌
본문내용
2. 실험 결과에 대한 고찰
본 실험에서는 용해 반응의 용해도곱 상수를 구하고, 공통 이온 효과를 확인해보았다. 본 실험에서 공통 이온으로 작용하는 이온은 이다. NaOH의 농도가 다른 4개의 용액을 만들어 비교하였는데, 공통 이온 효과에 의하면 초기 용액에 있던 의 농도가 클수록 의 용해도가 작아져야 한다. 이를 확인하기 위해 용액을 염산으로 적정하여 용액 중 의 총 농도를 구하였고, 이를 통해 가 녹아 생긴 의 농도를 구할 수 있었다. 실험 결과로부터 공통 이온 효과가 일어나는 것과 공통 이온 농도에 따라 영향을 받는 것을 확인해 볼 수 있었다. 또한 용해도곱 상수 역시 구할 수 있었다.
추가적으로, 농도가 다른 4가지의 NaOH 용액에서 걸러낸 용액의 온도가 조금씩 다른 이유는 NaOH가 용해되면서 발생한 열 때문이다. 실제 NaOH(s)→NaOH(aq) 반응의 ∆H=-44.5KJ/mol이므로 발열반응이다.참고자료
· 일반화학, Zumdahl, Chapter 13. Chemical Equillibrium태그
-
자료후기
-
자주묻는질문의 답변을 확인해 주세요

꼭 알아주세요
-
자료의 정보 및 내용의 진실성에 대하여 해피캠퍼스는 보증하지 않으며, 해당 정보 및 게시물 저작권과 기타 법적 책임은 자료 등록자에게 있습니다.
자료 및 게시물 내용의 불법적 이용, 무단 전재∙배포는 금지되어 있습니다.
저작권침해, 명예훼손 등 분쟁 요소 발견 시 고객센터의 저작권침해 신고센터를 이용해 주시기 바랍니다. -
해피캠퍼스는 구매자와 판매자 모두가 만족하는 서비스가 되도록 노력하고 있으며, 아래의 4가지 자료환불 조건을 꼭 확인해주시기 바랍니다.
파일오류 중복자료 저작권 없음 설명과 실제 내용 불일치 파일의 다운로드가 제대로 되지 않거나 파일형식에 맞는 프로그램으로 정상 작동하지 않는 경우 다른 자료와 70% 이상 내용이 일치하는 경우 (중복임을 확인할 수 있는 근거 필요함) 인터넷의 다른 사이트, 연구기관, 학교, 서적 등의 자료를 도용한 경우 자료의 설명과 실제 자료의 내용이 일치하지 않는 경우
찾으시던 자료가 아닌가요?
지금 보는 자료와 연관되어 있어요!
문서 초안을 생성해주는 EasyAI